振奋人心!8个国产重磅新药临床数据首发,涵盖老年痴呆、红斑狼疮、肿瘤......
来源:米内网 点击量:4374 时间:2019-09-30
金秋九月,金鸡湖畔。9月21日,第四届中国医药创新与投资大会正式拉开帷幕。在临床数据全球首发专场上,部分新药研发公司与业内专家对8个在研重磅新药的临床数据进行全球首发,涵盖阿尔兹海默症、系统性红斑狼疮、耐药菌、非肌层浸润性膀胱癌等治疗领域。披露的临床试验结果疗效显著,安全性高,这一振奋人心的结果让我们看到中国原研药更光明的未来。
GV-971:首个靶向肠道菌群的阿尔兹海默症新药
阿尔兹海默症(AD)又称老年性痴呆,是一种中枢神经系统变性病。截至目前全球约有5000多万患者,其中中国约有1000多万患者。由于AD的发病机制尚未明确,目前临床上以对症治疗为主,包括药物改善认知功能及记忆障碍、康复训练延缓病情进展等。
在过去的25年间,国际上药企们投入了6000多亿美元研发该领域治疗药物,但至今暂未有研发成果,截至目前约有320个药物研发失败,辉瑞、强生等大药企也纷纷表示,暂时退出现在研究领域。
据美国AD协会预测,假如现在有一款针对AD病因或缓解病情进展的新药获批上市,未来5年重度AD患者将减少50%,到2050年将减少80%。可见抗AD新药在全球具有迫切的临床需求。
GV-971是中国原创、国际首个靶向肠道菌群、降低神经炎症的抗AD药物,从发现至今,走过了漫长的22年。III期临床研究为36周、多中心、随机、双盲、安慰剂对照,有818例轻、中度AD患者随机入组。研究结果显示,GV-971以900mg/天连续治疗36周,主要疗效指标ADAS-cog量表相对安慰剂组改善2.54分,具有极其显著的统计学意义和临床意义,并且显示出持续改善的趋势。此外,GV-971对患者认知功能障碍也有改善作用。从安全性角度看,GV-971不良反应或严重不良反应事件发生率与安慰剂组无明显差异,安全性良好。GV-971如若研制成功,将填补该领域17年市场空白,惠及广大AD患者。
泰它西普:系统性红斑狼疮双靶点创新药物
系统性红斑狼疮(SLE)是一种多发于青年女性的,累及多脏器的自身免疫性炎症性结缔组织病,有致命的危险。据美国多地区及我国流行病学调查报告显示,SLE患病率分别为14.6-122/10万人、70/10万人,目前全球SLE患者大概有500多万,国内患者大概有100多万。
研究显示,SLE是一种与B细胞相关的自身免疫性疾病,而BLyS和APRIL是调控B细胞分化的关键因子,葛兰素史克的抗BLyS单抗-贝利木单抗于2011年3月获得FDA批准上市,是美国近60年来批准的唯一SLE新药。据米内网全球药物研发库,该产品自上市后全球销售额逐年上涨,2018年实现销售收入4.73亿英镑,同比增长26.13%。
泰它西普(RC18)是荣昌生物制药自主研发的靶向BLyS和APRIL的双靶标创新生物药物,具有全新的药物结构和作用机制,从发现至今已有11年。多中心、随意、双盲、安慰剂对照的IIb关键临床试验,开始计划240个病例,最后实际入组249个病例。结果显示该试验达到首要临床终点,高剂量治疗组48周SLE应答指数显著高于安慰剂组(79.2% VS 32%),安全性方面表现优异,病人耐受性良好。泰它西普有望成为满足系统性红斑狼疮巨大临床需求的一个first-in-class的药物。
康泰唑胺:无骨髓抑制毒性的抗耐药菌1类新药
耐药菌被认为是对人类危害最大的细菌,据统计,目前全球每年约有70万人死于耐药菌感染,如若不采取有效措施,预计到2050年,全球每年将约有1000万人死于耐药菌感染。耐药菌感染不仅成为人类健康的杀手,同时对经济也有很大的影响。据世界银行组织估计,如果耐药菌未得到有效控制的话,全球每年GDP将会下降3.8%。
耐药菌问题逐年恶化,但临床上可用于治疗耐药菌的新药却寥寥可数。康泰唑胺(MRX-1)是盟科药业自主研发的1类抗菌新药,属于新一代噁唑烷酮类抗菌药,用于治疗革兰氏阳性菌,包括耐甲氧西林金黄色葡萄球菌(MRSA)引起的感染。同类首个上市药物利奈唑胺由辉瑞开发,全球销售峰值超过13亿美元。
图:2013-2018年中国公立医疗机构终端利奈唑胺销售情况(单位:万元)
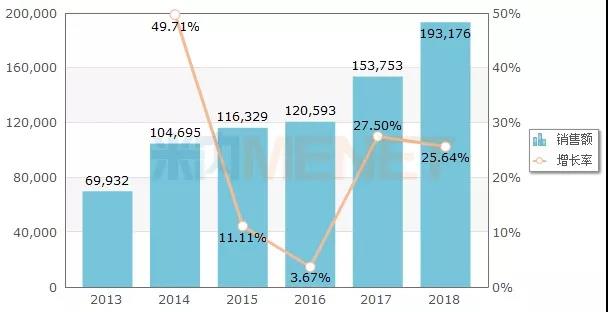
辉瑞的利奈唑胺(片剂及注射剂)于2006年进入国内市场,目前已有多个仿制药获批上市。据米内网数据,2018年中国公立医疗机构终端利奈唑胺的销售额为19.32亿元,同比增长25.64%,主要销售剂型包括片剂、注射剂、干混悬剂等。虽然近几年来国内抗生素总体市场逐年下滑,但针对耐药菌的新药销售额呈现上涨的态势。
虽然利奈唑胺治疗耐阳性菌疗效显著,但具有跟骨髓抑制相关的毒性,不能长期使用。盟科药业的康泰唑胺成功攻克了同类药物的骨髓抑制毒性,并且疗效显著。“以利奈唑胺为对照,MRX-1治疗复杂性皮肤和软组织感染成人患者的多中心随机双盲III期临床试验”结果显示,康泰唑胺临床疗效与利奈唑胺相当(临床治愈率93.0% VS 93.4%),但血液学不良事件显著低于利奈唑胺,具有更好的安全性优势,有望为耐药菌感染患者提供一种安全有效药物的选择。
APL-1202:全球首个口服治疗非肌层浸润性膀胱癌新药
膀胱癌虽然不像肺癌、乳腺癌那么高发,但在男性群体里发病率也是很高的,目前全球新生膀胱癌患者将近55万人,而中国将近有10万的新发病人。非肌层浸润性膀胱癌又称表浅性膀胱癌,指未在上皮内浸润性生长,没有形成内翻性乳头状瘤或浸润性癌的一类膀胱癌。
手术切除肿瘤是目前治疗非肌层浸润性膀胱癌的主要治疗方案,但术后复发率较高,为降低或预防术后复发,临床上会使用化疗药物或卡介苗进行灌注治疗,如果发生耐药,就需要进行膀胱全切手术。可见,目前非肌层浸润性膀胱癌在临床上有两个较大需求:一是已经复发耐药的患者如果没有有效的治疗药物,就得进行膀胱全切,大大降低生活质量;二是灌注治疗非常麻烦,患者依从性较差。
APL-1202作为全球首创的口服、可逆性的MetAP2抑制剂,既能抑制肿瘤细胞的成长,也能抑制肿瘤血管新生。开放性、多中心II期临床,针对化疗/卡介苗灌注失败的高危患者的研究结果表明,APL-1202的疗效显著优于目前的化疗灌注药物,中位无复发生存时间与现有药物相比提高一倍,药物使用安全、方便、毒副作用小。目前正在中国开展多中心的随机、双盲、安慰剂对照的注册临床研究,并在美国开展与卡介苗灌注联合用药的Ib临床研究,APL-1202有望成为全球首个非肌层浸润性膀胱癌口服治疗药物。
溶瘤病毒OH2注射液:肿瘤免疫治疗1类新药
重组溶瘤II型单纯疱疹病毒OH2注射液属于肿瘤疫苗和肿瘤基因治疗1类新药,有广谱及强效低毒的抗肿瘤疗效,主要针对实体瘤的治疗;也可与传统放化疗联合应用,提高疗效、降低副作用,同时还有预防和治疗转移瘤的效果。
溶瘤病毒在抗肿瘤方面有两方面的激励作用:一是溶瘤病毒可以选择性地在肿瘤细胞里面繁殖,发挥直接溶瘤作用,此外还可以诱发肿瘤细胞释放;二是溶瘤病毒可以携带免疫调控基因,在复制过程中可以表达这个调控基因,从而活化免疫细胞,可以对简单的转移瘤有很好的抑制作用。
武汉滨会生物科技开发的OH2注射液于2018年6月获批临床,已针对黑色素瘤、结直肠癌、肝癌、肺癌、乳腺癌、头颈部肿瘤等多个实体瘤开展I期临床试验。I期临床研究表明:OH2注射液安全性良好,研究者判断与药物可能有关的不良事件均程度较轻,受试者均未出现剂量限制性毒性(DLT);初步显示出良好的抗肿瘤效应,总体疾病控制率(DCR)为78%;受试者血液、唾液、尿和粪便中均未检测出OH2病毒拷贝数。
Oregovomab:原发卵巢癌一线治疗性疫苗
原发性卵巢癌是一种死亡率较高的女性生殖系统疾病,在女性常见恶性肿瘤所占比例为2.4%-6.5%,在女性生殖系统疾病患病率排位第三,仅次于宫颈癌和宫体癌。
原发性卵巢癌传统治疗方法为手术+卡铂/紫杉醇,2014年取得突破性进展,FDA批准了2款新药上市,分别为罗氏的安维汀(贝伐珠单抗注射液)以及阿斯利康的PARP抑制剂奥拉帕利。据米内网全球药物研发库,2018年贝伐珠单抗及奥拉帕利全球销售额分别为68.49亿瑞士法郎、6.47亿美元。
目前治疗原发卵巢癌的药物仅适用于卡铂敏感且伴有BRCA基因突变的患者,昂瑞生物医药研发的Oregovomab(OV)是针对肿瘤抗原CA125的单克隆鼠源抗体,通过与一线化疗(SOC)精准联合治疗,启动对表达CA125抗原肿瘤细胞的系列免疫反应。全球多中心针对晚期原发卵巢癌III/IV期(入组100例病人)IIb临床试验,36个月临床终点取得超出预期的临床疗效,相对标准化疗SOC方案,OV与SOC联合用药,PFS从13.3月增加到41.8月;OS为21人死亡(SOC化疗组)vs 8人死亡(SOC+OV),两组之间的不良事件、严重不良事件的发生率无明显差异。OV与SOC的联合有可能成为原发卵巢癌的一线治疗药物。
TAA013:国内首个乳腺癌抗体偶联药物
乳腺癌在国内外都是女性面临的首要恶性肿瘤,目前全球每年新发病例达到167.1万,死亡病例达到52.2万,其中有约25%的患者为HER2阳性乳腺癌。目前国内治疗HER2阳性乳腺癌的常用药物为罗氏的曲妥珠单抗(赫赛汀),据米内网数据,2018年中国公立医疗机构终端赫赛汀的销售额为39.69亿元,同比增长51.35%。
TAA013是东曜药业开发的重组人源化抗HAR2的单克隆抗体(曲妥珠单抗),通过链接SMCC与微观抑制剂DM1,共架链接而成的抗体偶联药物(ADC),ADC通过反向特定抗原有效渗透到肿瘤组织,并被肿瘤细胞吞噬进入融媒体,释放效应分子,杀伤肿瘤细胞,目前已成为肿瘤研究的重点方向和热门之一。
目前I期临床试验结果证实TAA013是可耐受且安全有效的,在接受过多种抗HER2药物治疗的HER2阳性乳腺癌患者中看到初步疗效。目前国内尚无治疗HER2阳性乳腺癌患者的抗体偶联药物上市,TAA013有望成为首个。
CAN008:国内首个胶质母细胞瘤创新靶向药
胶质母细胞瘤(GBM)是一种比较常见的、恶化程度高、死亡率高、愈后效果差的新型脑细胞瘤,发病率约为3.1/10万人。传统的标准疗法是放射疗法加上TMZ,但治疗效果不是很好,1年总体生存率37.2%,5年总体生产率只有5.1%。
CAN008(CD95受体/Fc融合蛋白)是北海康成制药开发的我国首个进入GBM临床ll/III期研究的I类创新靶向生物药,是一种具有双重作用机制的CD95L抑制剂。目前已获得FDA和EMA的罕用药资格认定,EMA快速审评资格认定等。
CAN008于2019年初在台湾完成的I期研究结果显示,新诊断GBM患者接受CAN008联台标准RT/TMZ治疗具有良好的安全性和耐受性,400mg/周剂量的疗效令人鼓舞,PFS6到达了57.1%。
来源:第四届中国医药创新与投资大会、米内网数据库


