血清药理学方法观察复方斑蝥胶囊对 人肝癌细胞SMMC-7721增殖的影响
来源:信息员 点击量:5850 时间:2016-06-29
血清药理学方法观察复方斑蝥胶囊对人肝癌细胞SMMC-7721增殖的影响
杨军 ,丁敏 ,张太君,宋自阆,曹永艳
摘要
目的:研究复方斑蝥胶囊含药动物血清对人肝癌细胞SMMC一7721增殖的影响。方法:采用血清药理学方法,对兔灌胃给予不同剂量(临床等效剂量、2倍临床等效剂量和3倍临床等效剂量)的复方斑蝥胶囊混悬液,应用MTT比色法观察含药血清对人肝癌细胞SMMC一7721增殖的抑制作用,同时观察临床等效剂量组各采血时间点的抑制作用。结果:3个剂量组的含药血清对SMMC一7721细胞增殖均有抑制作用(P<0.01),其中以3倍临床等效剂量组合药血清的抑制率最高;临床等效剂量组各采血时间点的含药血清对SMMC一7721细胞增殖均有抑制作用(P<0.05),其中3h时含药血清的抑制率最高。结论:复方斑蝥胶囊含药动物血清对人肝癌细胞SMMc一7721增殖具有一定的抑制作用,并具有剂量依赖性。
关键词 复方斑蝥胶囊;人肝癌细胞SMMC一7721;血清药理学复方斑蝥胶囊(FBC)的主要成分有斑蝥、熊胆粉、人参等,临床上主要用于治疗癌症,尤其是对原发性肝癌,显示了较好的疗效。该药杀灭肝癌细胞的机制在国内、外还未见相关报道,为此,笔者采用血清药理学方法观察家兔灌胃给予复方斑蝥胶囊后其含药血清对人肝癌细胞SMMC一7721增殖的影响,以为复方斑蝥胶囊治疗肝癌提供实验依据。
1 材料与方法
1.1 动物与试药
新西兰大耳白兔15只,体重(2.5±0.2)kg,雌雄不限,由重庆医科大学实验动物中心提供,许可证号:SCXK(渝)20020001。噻唑蓝(MTT)、二甲基亚砜(DMSO)(美国Amresco公司);RPMI1640培养基、胰蛋白酶(美国GIBCO公司);FBC。
1.2 细胞
人肝癌细胞SMMC一7721由重庆医科大学基础医学院病理生理教研室惠赠。处理方法:将细胞株培养于含10%胎牛血清的RPMI1640培养液中,置于37℃ 培养箱中,在5%CO 、饱和湿度条件下培养,2d~3d后以0.1%胰酶消化传代。
1.3 最佳采血时间点的确定
取兔3只,体重(2.5±0.1)kg,雌雄不限。以FBC内容物临床等效剂量加入磷酸盐缓冲液(PBS)制成混悬液后灌胃给药,1次/d,连续3d,末次给药后1、2、3、4、5h自耳缘静脉采血,分离血清,56℃灭活30min,O.22um滤膜过滤,除菌,-20~C保存,备用。对照血清于给药前采血制备,方法同含药血清。将各兔相应时间点含药血清等量混合。以各采血时间点的含药血清进行MTT试验。以确定最佳采血时间点。
1.4 分组及中药悬液制备
将兔分为临床等效剂量组(n=6)、2倍临床等效剂量组(n=3)和3倍临床等效剂量组(n=3)。临床等效剂量组的给药剂量=临床用量×等效剂量系数(按体表面积计算)×培养体系血清稀释度 。动物体表面积和体重之间的关系通用公式:lgS=0.8 762+0.698lgW。式中S为体表面积(cm),W 为体重(g),人标准体重按70kg计算 。复方斑蝥胶囊的临床用量为1500mg/d,等效剂量系数=S兔/ S人,培养体系血清稀释度为1O。以适量PBS将FBC内容物制成混悬液。其它剂量组按相应倍数加倍。将上述3组兔灌胃给予相应药物后(1次/d,连续3d),于末次给药后3h自耳静脉取血,分离血清,制作含药兔血清;将给药前的兔(n=3)以同样方法分离血清作为对照兔血清组。另制备空白对照组(不加细胞,只加培养液)和细胞对照组(不加兔血清,作为各处理组各浓度水平的共同对照)。
1.5 MTT试验
取对数生长期人肝癌细胞SMMC一7721,消化,以PBS洗涤2次。离心,弃去上清液,用含10%胎牛血清的RPMI1640培养液配成浓度为1.5×104 个/ml的细胞悬液。将此细胞悬液接种于96孔板,每孔接种180ul,培养24h后加入相应对照兔血清或含药兔血清20u1,细胞对照组加入ul PBS,每孔设8个复孔。继续培养48h后小心吸出培养液,换以l80 ul不含胎牛血清的RPMI1640培养液和20ulMTT,置于5%C02、37℃培养箱中继续培养4h,吸去培养液,加入200 ul DMSO,振荡10min,使结晶充分溶解。在酶联免疫检测仪上测定吸光度值,测定波长为570nm。
抑制率=(对照血清组A值一实验血清组A值)/对照血清组A值。
1.6 剂量一反应曲线
取兔12只,体重(2.5±0.1)kg,雌雄不限,分为临床等效剂量组、2倍临床等效剂量组、3倍临床等效剂量组和对照组,每组3只。各组以相应剂量FBC内容物悬液对兔灌胃给药,1次/d,连续3d,于末次给药后最佳采血时间点采血,分离血清,56℃灭活30min,0.22um滤膜过滤,除菌,-20℃保存,备用。对照组除以等体积PBS灌胃外,其余操作均同含药组。将各组内3只兔的血清等量混合,进行MTT试验,绘制剂量---反应曲线。
1.7 统计学方法
结果以 EQ 开关参数 x(_)±S表示,并进行方差分析和SNK(Student—Newman—Keuls)检验。
2 结果
2.1 不同采血时间点血清MTT试验结果以临床等效剂量组不同采血时间点含药血清进行MTT试验,结果详见表1和图1。
表1 不同采血时间点MTT试验结果(A,x(_) ±s)
Tab 1 Results of M TT assay with drug sera collected
atdifferent hours(A,x(_)±s)
|
细胞对照组 |
对照血清组 |
FBC临床等效剂量组 |
||||
|
1 h |
2h |
3h |
4h |
5h |
||
|
1.138± 0.072 |
l.135± 0.086▲ |
0.950± 0.174* |
0.915± 0. O95* |
0.820±0.100*Δ |
0.896±0.072* |
1.109±0.098# |
与细胞对照组比较:▲P>0.05;与对照血清组比较:*P<0.Ol,#P<0.05;与5h时间点比较:△P<0.05
Compared with the cellular control group:▲P >0.05;comparedwith the rabbit serum group:*P <0.01,#P<0.05;compared with the serum at 5hr:△P <0.05
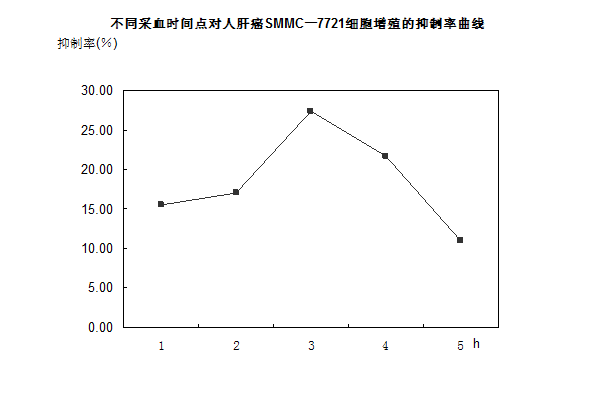
图1 不同采血时间点对人肝癌SMMC一7721细胞增殖的抑制率曲线
Fig 1 Inhibitory rate curves on SM MC 。。7721 cells proliferation
with drugs sera collected at different hours inclinical equivalent dose group
由表1可见,对照血清组与细胞对照组比较,吸光度无显著性差异(P>0.05),说明未含药的对照血清对人肝癌SMMC一7721细胞增殖无抑制作用。
由图1可见,各取血时间点的含药血清对SMMC一7721细胞增殖均有抑制作用。5h时吸光度与对照组吸光度比较具有显著性差异(P<0.05),其余各时间点吸光度与对照组吸光度比较具有极显著性差异(P<0.01);3h时间点的吸光度与5h时间点的吸光度比较具有显著性差异(P <0.05);其它各时间点之间两两比较无显著性差异(P>0.05)。1h~5h时间点含药血清对SMMC一7721细胞增殖抑制率由低到高再到低,在3h处达到峰值,因此最佳采血时间点确定为给药后3h。
2.2 不同剂量组血清MTT试验结果
以各剂量组含药血清进行MTT试验,结果详见表2和图2。
表2 不同剂量组MTT试验结果(A, x(_)±s)
Tab 2 Results of M TT assay with drug sera in different
dose groups(A, x(_)±s)
|
细胞对照组 |
对照血清组 |
FBC等效剂量组 |
FBC2倍等效剂量组 |
FBC3倍等效剂量组 |
|
1.136±0.082 |
1.132±0.068 |
0.800±0.080 |
0.735±0.058 |
0.658±0.135 |
与细胞对照组比较:▲p>0.05;与对照血清组比较:* P<0.01;与等效剂量组比较:△P<0.01
compared with the cellular control group:▲p > 0.05;comparedwith the rabbit serum group:*P<0.01;compared with the clinicalequivalent group:△P< 0.01
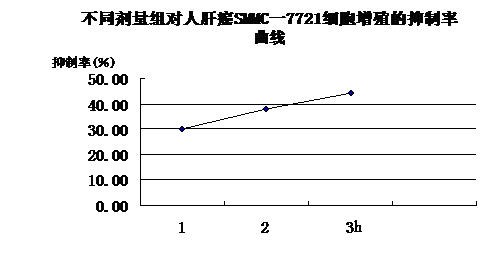
图2 不同剂量组对人肝癌SMMC一7721细胞增殖的抑制率曲线
Fig 2 Inhibitory rate curves on SM MC 。。7721 cells proliferationwith drug sera collected in different dose groups
由表2和图2可见,对照血清组与细胞对照组比较,吸光度无显著性差异(P>0.05),说明对照血清对SMMC一7721细胞增殖无抑制作用。FBC各剂量组血清对SMMC一7721细胞增殖均有抑制作用,吸光度与对照组比较有极显著性差异(P<0.01)。其中,3倍等效剂量组与等效剂量组比较,吸光度具有极显著性差异(P<0.01)。提示含药血清对SMMC一7721细胞增殖存在着剂量依赖性抑制作用。
3 讨论
传统的中药药理体外实验是将未精制提取的中药或中药复方粗制剂直接加入离体反应体系(细胞培养、酶反应)中进行的,难以获得与体内药物作用相同的结果。日本学者“在20世纪80年代提出血清药理学的概念,即给动物灌服受试药物,在一定的时间里,取其血清进行实验。已有众多研究表明,采用血清药理学方法研究复方中药的药理作用具有一定的科学性和合理性。血清药理学理想的采血时间应为血药浓度达到峰值左右的时间,这样能够避免因有效物质尚未吸收或代谢完全而造成的假阴性结果。多数学者认为,不同研究中的最佳采血时间应当通过实验来确定。笔者通过比较不同时间点的含药血清对SMMC一7721细胞抑制率的结果,确定以末次给药后3h为最佳采血时间点。在应用血清药理学研究复方中药的药理作用过程中,由于加入反应系统的血清需经稀释后使用,故应尽可能增大给药剂量。但给药剂量加倍后,血药浓度却不可能也增加相应倍数,因为血药浓度与给药剂量并不成等比增加,同时还要受到灌胃药物浓度和体积的限制。鉴于此,笔者在本研究中采用王力倩等提出的参考公式确定了给药剂量,并且在此基础上增加了2个剂量组。结果表明,复方斑蝥胶囊含药血清对SMMC一7721细胞增殖存在剂量依赖性抑制作用。通过实验,笔者确定了制备复方斑蝥胶囊含药血清的最佳采血时间和给药剂量,为以后应用血清药理学的方法研究复方斑蝥胶囊的分子药理学作用机制奠定了基础。
参考文献
【1】曲震,史彦芬,王义善.HLF方案合并复方斑蝥胶囊治疗原发性肝癌30例近期疗效观察【J】.中国中医药科技,2002,9(6):336.
【2】 王力倩,李仪奎.血清药理学方法研究探索【J】.中药药理与临床,1997,13(3):29.
【3】袁博俊,王治乔.新药临床前安全性评价与实践【M】.北京:军事医学科学出版社,1997:48.
【4】Hiroko 1wama,Sakae Amagaya,Yukio Ogihara.Effectof shosaikoto,a Japanese and Chinese traditional herbalmedicinal mixture,on the mitogentic activity of lipopolysaccharide:a new pharmacological testing method【J】.J Ethmopharmacol,1987,21(1):45.
【5】余文珍.复方中药含药血清研究现状【J】.中医药通报,2003,2(2):113.
【6】谢华,贾正平,徐丽婷,等.瑞香狼毒水提物小鼠的药物血清对K562细胞增殖的影响【J】.中国药房,2001,12(7):400.
【7】李仪奎.中药血清药理学实验方法的若干问题【J】.中药新药与临床药理,1999,10(2):95.
【8】包金凤,刘国卿.中药血清药理学的方法学研究概述【J】.药学进展,2000,24(2):89.
中国药房 2005年第16卷第4期


